#원자에 대한 모든 것#입자설#원자설#돌턴의 원자설#원자의 특징#원자 모형#원자의 구조#원자 모형의 변천
고대의 입자설
학자:데모크리토스
내용:뮬질은 더 이상 쪼갤수 없는 입자 즉 원자로 이루어져있다.
자연 현상:입자와 입자 사이의 빈 공간이 존재한다.
→공기를 압축하면 공기를 이루는 입자 사이의 거리가 가까워진다.
증거:1,물100ml와 에탄올100ml을 섞으면 200ml보다 적다.(입자 사이의 거리가 존재하기 때문에)
2,금속박을 무한히 얇게 만들거나 비눗방울을 무한히 크게 만들 수 없다.
3,물에 붉은색 잉크를 떨어뜨리면 물 전체로 퍼진다.
고대의 연속설
학자:아리스토텔레스
내용:물질은 연속적이며 무한히 쪼갤 수 있고 계속 쪼게면 결국 사라진다.
자연현상:자연은 진공을 싫어하며 물질 사이의 빈 공간은 존재하지 않는다.
→공기를 압축하면 공기가 진해진다.
증거: 입자설 보다 많이 적다.(따로 배우지 않음)
돌턴의 원자설
| 1,물질은 더이상 쪼갤 수없는 원자로 구성되어 있다 | 2,원자의 종류가 같으면 질량과 무게도 같다. |
| 3,원자는 없어지거나 새로 생기지 않고 다른 종류의 원자로 변하지 않는다. | 4, 서로 다른 원자들이 일정한 비율로 결합해서 새로운 물질을 만듬 |
|
|
돌턴의 원자설 수정
-원자는 중성자와 양성자로 나눌 수 있다.
-같은 원자라도 질량이 다른 동위 원소가 발견됨(예:수소, 중수소, 삼중수소)
-원자는 핵반응에 의해 다른 원자로 바뀔 수 있다(예:하지만 화학반응으로는 불가능)
원자
meaning:물질을 구성하는 기본 입자
| 구분 | 원자 | 원소 |
| 정의 | 물질을 구성하는 입자 | 물질을 구성하는 성분의 종류 |
| 특징 | 원소를 구성하는 실제 입자 개수를 셀 수 있다 | 같은 종류의 원자를 통틀어서 부르는 집합 |
| 비유 | 개수를 나타내는 것 | 종류를 나타내는 것 |
원자의 구조
| 원자핵 | 전자 |
| 1,전하를 뛰고 있다 2,원자의 중심 3,전하를 띠는 양성자와 중성자로 이루어져있다 4,원자질량의 대부분을 차지함 |
1,전하를 띠고 있다 2,원자핵 주위를 돌고 있다 3,원자핵에 비해 질량이 매우 작음 |

입자의 특징
원자는 종류에 따라 different(원자의 종류에 따라 양성자 수가 다름)
원자는 전기적인 중성임(원자의 전하량=원자핵)
원자의 크기와 질량
원자의 질량은 대부분 원자핵이 차지하며, 전자의 크기와 질량은
무시할 수 있을 정도로 작음
원자 모형
meaning:원자는 매우 작기 때문에 원자 구조를 설명하기 위해 나타내는 모형
| 구분 | 혤륨 원자 | 리튬 원자 | 산소 원자 |
| 모형 | |||
| 원자핵 전하 | 2 | 3 | 8 |
| 전자 수 | 2 | 3 | 8 |
원자모형의 변천
1. 돌턴(1803)의 원자 모형
▶ 물질은 더 이상 쪼갤 수 없는 공 모양의 딱딱한 원자로 이루어져 있음

▶ 특징
- 화학의 기본 법칙(질량 보존 법칙, 일정 성분비 법칙, 배수 비례 법칙) 설명의 이론적 토대 수립
▶ 한계점
- 톰슨의 음극선 실험 결과 설명 불가능
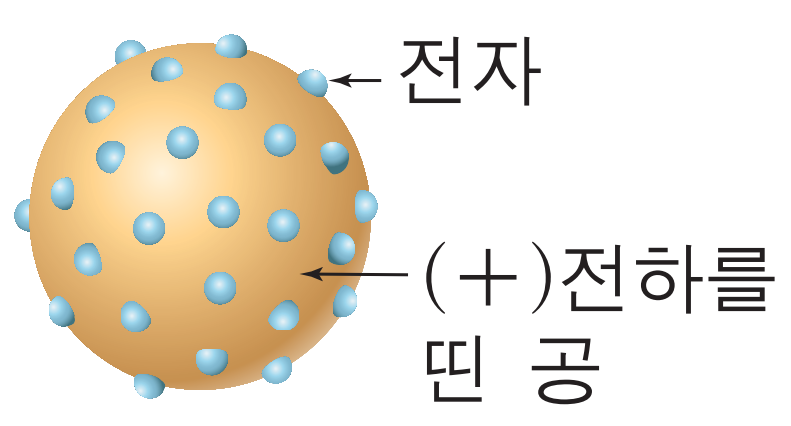
2. 톰슨(1897년)의 원자 모형
▶ (+)전하를 띤 부드러운 공 속에 (-)전하를 띤 전자가 드문드문 박혀 있음
▶ 특징
- 원자가 고른 밀도를 가진 (+)전하를 띤 공 속에 (-)전하를 띤 전자가 박혀 있다고 주장하여 원자의 전기적 성질을 일부 설명함
▶ 한계점
-
러더퍼드의 알파 입자 산란 실험 결과 설명 불가능
3. 러더퍼드(1911년)의 원자 모형
▶ 원자의 중심에 크기가 매우 작고 질량이 큰 (+)전하를 띤 원자핵이 있고, 그 주위를 (-)전하를 띤 전자가 돌고 있음

▶ 특징
- 원자의 중심에 있는 원자핵의 존재 및 원자핵의 성질과 원자가 대부분 빈 공간임을 밝힘
▶ 한계점
-
수소의 선 스펙트럼 설명 불가능
4. 보어(1913년)의 원자 모형
▶ 원자핵을 중심으로 전자는 일정한 에너지를 가지는 원형의 궤도를 돌고 있음

▶ 특징
- 수소 원자의 선 스펙트럼 설명 가능
▶ 한계점
-
2개 이상의 전자를 가지는 다전자 원자의 선 스펙트럼 설명 불가능
5. 현대의 원자 모형
▶ 원자핵 주위에 전자가 발견될 확률만을 알 수 있으며, 확률 분포를 구름과 같은 모양으로 나타냄

▶ 특징
- 슈뢰딩거(1926년): 특정 위치에서 전자가 발견될 확률을 계산→ 확률 분포를 구름처럼 나타내는 전자 구름 모형 제시
- 채드윅(1932년): 중성자의 존재 확인→ 원자핵은 양성자와 중성자로 이루어짐
▶ 한계점
-
점은 전자의 개수를 의미하는 것이 아니라 전자가 존재할 수 있는 확률 분포를 나타냄